查看更多
密碼過期或已經(jīng)不安全,,請(qǐng)修改密碼
修改密碼
壹生身份認(rèn)證協(xié)議書
同意
拒絕

同意
拒絕

同意
不同意并跳過






本期看點(diǎn)
在第48周時(shí),Survodutide治療組中高達(dá)90%的患者實(shí)現(xiàn)了≥30%的肝臟脂肪含量 (LFC) 減少,。其他指標(biāo)如增強(qiáng)肝纖維化 (ELFTM) 評(píng)分,、FAST評(píng)分、PRO-C3,、ALT,、AST水平以及體重均較安慰劑組改善。
在安全性方面,,Survodutide治療組和安慰劑組的任何治療期間出現(xiàn)的不良事件發(fā)生率相似,,胃腸道事件是最常報(bào)告的不良事件,未發(fā)現(xiàn)新的安全性問題,。
編者按
黃煒燊教授做大會(huì)口頭報(bào)告
2025年3月28日,,在第34屆亞太肝病學(xué)會(huì)年會(huì)(APASL 2025)上,我國香港中文大學(xué)黃煒燊(Vincent Wai-Sun Wong)教授進(jìn)一步報(bào)告了該項(xiàng)全球多中心,、雙盲,、II期臨床試驗(yàn)中,來自東亞患者人群的亞組分析結(jié)果(大會(huì)編號(hào):OP0013),。此次報(bào)告進(jìn)一步揭示了Survodutide在東亞MASH伴纖維化患者中的療效和安全性,。
研究背景
GCGR/GLP-1R雙重激動(dòng)劑同時(shí)兼具促進(jìn)胰島素分泌、降低血糖,、抑制食欲等GLP-1R激動(dòng)劑的作用,,以及增加能量消耗、直接改善肝臟脂肪酸氧化,、脂肪代謝等激活GCGR的獨(dú)特效應(yīng),,在MASH全程管理中的價(jià)值愈發(fā)突顯。此次亞組分析聚焦東亞人群,,評(píng)估GCGR/GLP-1R雙重激動(dòng)劑Survodutide在東亞MASH伴纖維化患者中的療效及安全性,。
研究方法
該項(xiàng)II期臨床試驗(yàn)共納入295例經(jīng)活檢證實(shí)MASH伴肝纖維化(NAS評(píng)分≥4、肝纖維化分期為F1-F3期),,且體重指數(shù)(BMI)≥25 kg/m2的成人受試者,。隨機(jī)分配至每周一次皮下注射2.4 mg、4.8 mg或6.0 mg的Survodutide或安慰劑治療(24周內(nèi)逐步增加劑量),。
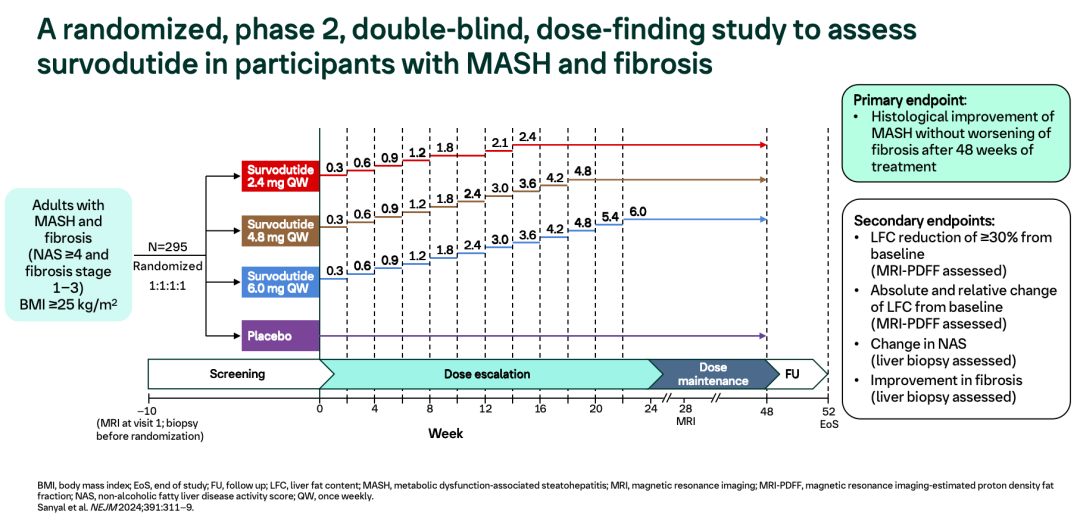
本次研究報(bào)告了東亞亞組,,包括來自中國內(nèi)地、中國香港,、中國臺(tái)灣,、日本、韓國的61例受試者的分析結(jié)果。主要研究終點(diǎn)為治療48周時(shí),,實(shí)現(xiàn)肝臟脂肪含量 (LFC,,基于MRI-PDFF評(píng)估)較基線水平減少≥30%的患者比例,其他研究終點(diǎn)包括增強(qiáng)肝纖維化(ELFTM)評(píng)分和肝酶(ALT,、AST)水平的絕對(duì)變化,;FAST評(píng)分、PRO-C3,、LFC以及體重的相對(duì)變化,。主要分析基于不同治療集實(shí)際治療集(Actual treatment)和計(jì)劃治療集(Planned treatment)。
研究結(jié)果
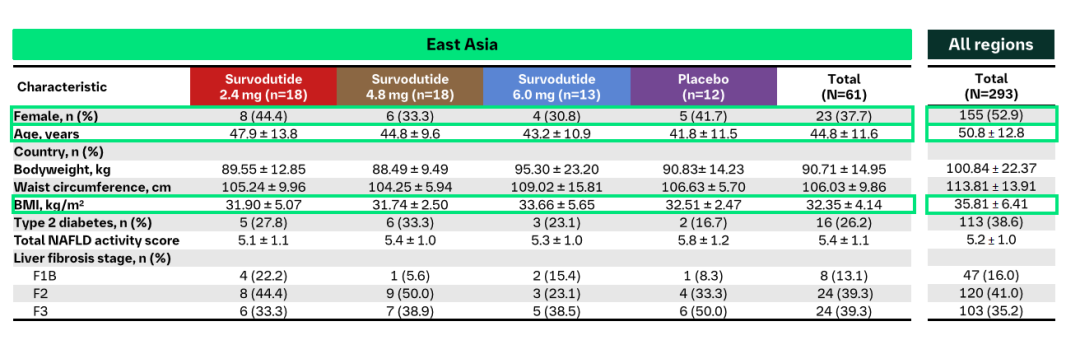
總體而言,,各治療組受試者基線特征與安慰劑組相似,。平均年齡44.8±11.6歲,女性占37.7%(23/61),,BMI平均值32.35±4.14 kg/m2,。相較于全人群患者,東亞亞組患者更年輕,,男性更多,,BMI和腰圍較低。而2型糖尿病的患病率,、基線組織學(xué)嚴(yán)重程度(包括NAS和纖維化分期)與全人群患者類似(表1),。
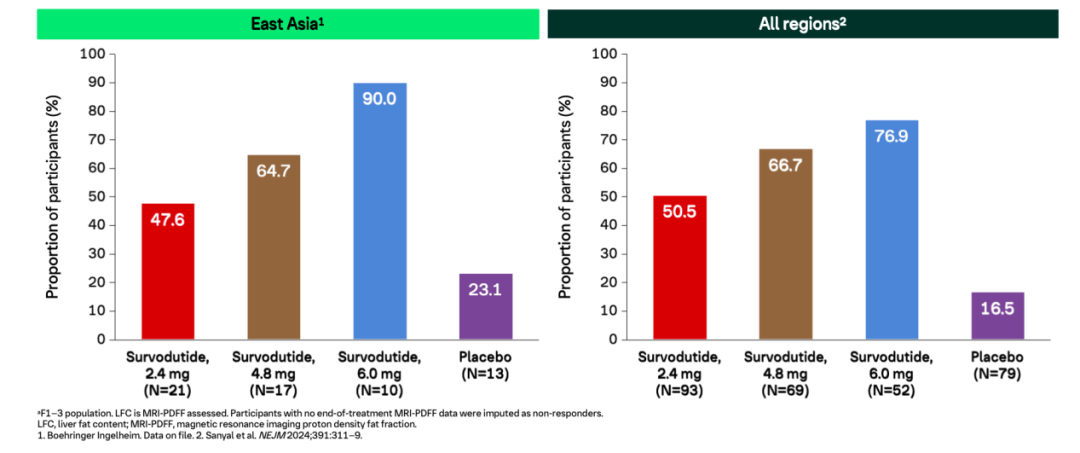
東亞亞組的分析結(jié)果顯示,在第48周時(shí),,Survodutide治療組中高達(dá)90%的患者實(shí)現(xiàn)了≥30%的LFC減少,,安慰劑組為23.1%,在數(shù)值上略高于全人群患者,。
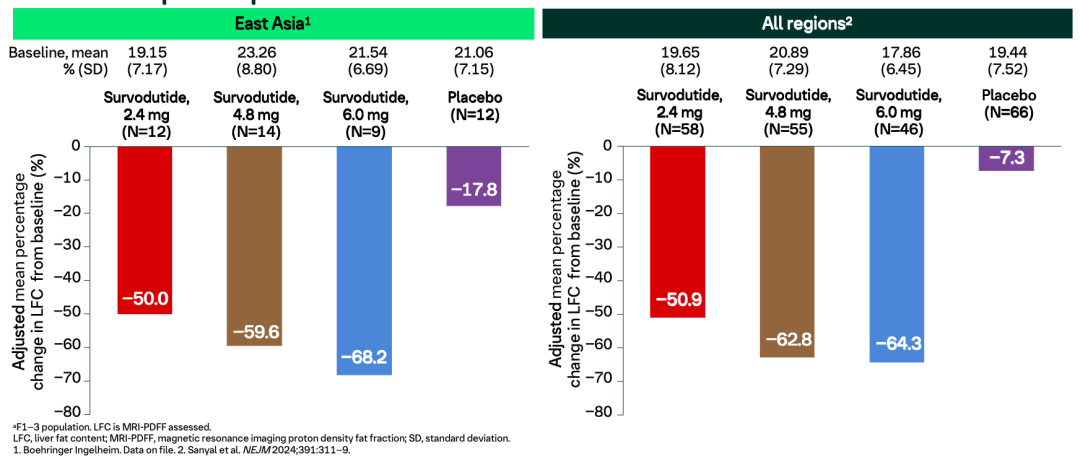
在第48周時(shí),Survodutide 2.4 mg,、4.8 mg和6.0 mg治療組患者的LFC的相對(duì)降低幅度分別為50.0%,、59.6%和68.2%,而安慰劑組為17.8%(圖3),。
經(jīng)過48周的治療,Survodutide使患者的ELFTM評(píng)分絕對(duì)值最高可降低0.89,,所有三個(gè)劑量組的ELFTM評(píng)分均降低超過0.5,。此外,Survodutide組在PRO-C3,、FAST評(píng)分,、ALT、AST以及體重等方面的改善也均優(yōu)于安慰劑組。其中,,PRO-C3最高可降低37.6%,,F(xiàn)AST評(píng)分最高可降低83.1%,ALT水平降低70.1 U/L,,AST水平降低36.6 U/L,;以上均與全人群患者相似。在體重方面,,東亞亞組的體重減輕最高達(dá)16.1%,,而全人群患者為13%。
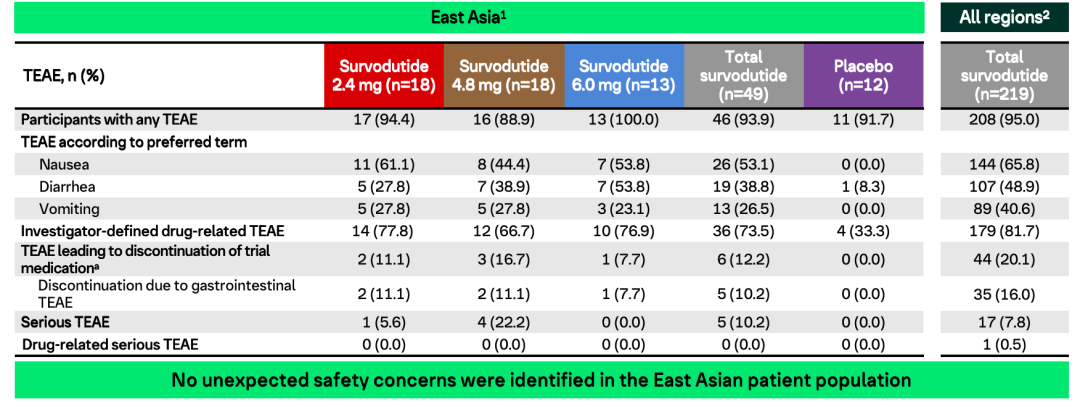
在安全性方面,,Survodutide治療組和安慰劑組的任何治療期間出現(xiàn)的不良事件發(fā)生率相似(圖4),,最常報(bào)告的不良事件為胃腸道不良事件,在東亞患者群體中未發(fā)現(xiàn)新的安全性問題,。相較于全人群患者,,東亞亞組惡心、嘔吐的發(fā)生率更低,。而且高劑量組中未出現(xiàn)嚴(yán)重不良事件,。這表明Survodutide在東亞MASH伴纖維化患者中具有良好的安全性和耐受性。
研究結(jié)論
此次APASL 2025大會(huì)報(bào)告的亞組分析結(jié)果證實(shí)了Survodutide在治療東亞MASH伴纖維化患者中的療效和安全性,,與總體人群研究的結(jié)果相一致。研究表明,,Survodutide治療48周,,能夠降低東亞患者的肝臟脂肪含量(LFC),改善肝酶,、各類纖維化相關(guān)的無創(chuàng)生物標(biāo)志物指標(biāo)(ELFTM,、PRO-C3、FAST評(píng)分),,且降低體重,。
會(huì)場花絮
調(diào)研問題
審批號(hào):SC-CN-16640
有效期至:2026年3月31日
僅供相關(guān)醫(yī)藥專業(yè)人士進(jìn)行醫(yī)學(xué)科學(xué)交流
PART
↓↓↓
查看更多